ROS1融合突变和靶向药物
+ A7 h1 Z1 M% XROS1融合突变和靶向药物
' G* H3 f: D" o. i% s' f: b2 nROS1基因也是肺癌中经常被提及的基因突变,但是其突变频率并不是特别高。另外很多患者和家属没有分清楚ROS1的突变形式,很多不靠谱的基因测序公司,对于ROS1基因上一个位点的突变都解析是药物敏感突变,对患者的靶向用药产生了极大的干扰。本帖注重对ROS1的基因突变形式、对应的靶向药物做一次系统梳理。
. r) t& R' {+ ?1: q0 O; [& a3 E5 t8 `" X( r
认识ROS1基因和其突变
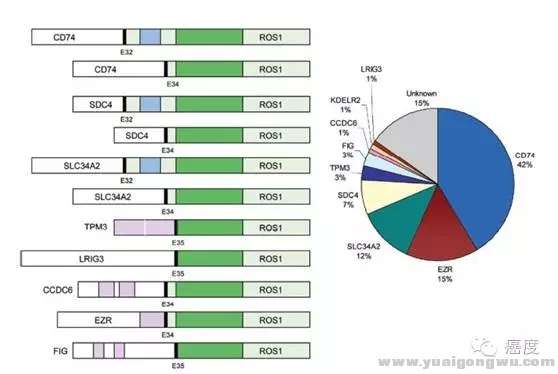
( ^" e* ^! n# h5 b; I0 ~ROS1基因的重排最开始是在人脑胶质瘤细胞系里被鉴定出来,后续在其他几个恶性肿瘤里也发现了ROS1基因的重排,如胆管癌、卵巢癌、胃癌和非小细胞肺癌,其中在非小细胞肺癌里的突变频率为1%-2%。ROS1基因可与多个基因发生融合突变,其中最主要的融合伴侣是CD74,(见下面图片),ROS1与其他基因发生融合时,一般会保留激酶结构域,而且在断裂点上较为保守。ROS1的重排导致激酶持续激活,上调SHP-1、SHP2以及PI3K、AKT、mTOR、MAPK和ERK信号通路,导致细胞持续增殖,肿瘤发生。3 I% A1 `6 P. R4 {
 7 i, c, ~2 U- f- l8 m5 [
7 i, c, ~2 U- f- l8 m5 [
图1:非小细胞肺癌中ROS1基因的融合形式$ a. W- M6 _, n- w9 f6 v9 G' Q( G1 d# A
上图是ROS1基因的融合形式,左侧的绿色部分为ROS1的酪氨酸激酶结构域,蓝色部分为跨膜结构域。右侧部分是报道的与ROS1发生融合变异的基因和其频率。由于存在多种基因可能与ROS1基因发生融合,因此在选择检测ROS1的变异时,需要着重技术原理,避免漏检。检测ROS1突变的技术有FISH(原位免疫荧光杂交)、RT-PCR(逆转录PCR)、IHC(免疫组化)和新一代测序(NGS)。目前FISH是ROS1融合的金标准,通过红色和绿色荧光探针标记ROS1基因两端,如果ROS1基因没有发生断裂,那么红绿荧光凑在一起表现为黄色荧光信号。如果ROS1基因中间发生了断裂,则可以观察到红色荧光、绿色荧光信号的分离,如果大于15%的肿瘤细胞呈现出这种分离信号,则判断为ROS1基因融合突变阳性。
( F) N8 R, d, A. s" V" ^

7 ]' i& t, ]6 \) H- }图2:FISH检测ROS1基因的重排- C: V- d1 M: @2 x" {
需要认识到任何检测技术都不是完美的,FISH的优势是可以检测石蜡切片组织(FFPE),这是RT-PCR不能具备的,RT-PCR对样本的RNA要求较高,需要新鲜的组织样本提取RNA才能进行逆转录。另外FISH还可以检测一些未知的融合突变,即不需要知道ROS1基因的融合伴侣是谁,只要ROS1发生分离了就行。缺点是手续繁琐、对试验员的操作要求较高。另外FIG基因在ROS1上游134kb处,因此FIG-ROS1的融合形式在荧光信号分离上不是很好判断。最关键的是FISH不能提供出和ROS1发生融合的伴侣基因是什么,是否有生物学和临床的意义。
7 n0 J5 r$ Y% k5 v% CRT-PCR因为需要之前设计引物,所以不能检测未知的融合突变形式。对样本的RNA要求较高,石蜡标本里RNA降解很严重。因此如果您的检测报告表明是RT-PCR检测的融合突变,而您的标本是石蜡标本,那么就需要注意是否存在假阴性的情况,不管是ALK或者ROS1以及RET都是这种情况。RT-PCR的优势是快速、样本需求量少。1 ^4 k; R) b# l+ u8 H; e, w: T% T: |
ROS1的免疫组化检测特点是简单,易操作。但是对抗体的要求较高,另外易受到染色背景、判读标准的影响,也有很多地方亟待提升。总之对于ROS1基因的融合突变,最好使用两种以上的检测技术进行相互验证,没有一项技术是可以做到100%的承诺的保证的,但是对于患者来说,漏检因为所有的希望。1 v, J; I) M; E1 q4 j
2
, D# M! x1 X4 k G& YROS1的患者和病理特点5 b3 Q5 v0 f2 |
ROS1融合突变是非小细胞肺癌的一个亚型(突变频率1%-2%),ROS1的患者群与ALK突变的患者拥有一些共同的特征,患者的特点是年轻、非吸烟、亚裔、进展较快。尽管ROS1融合突变也在肺大细胞癌、鳞状细胞癌里被鉴定出来过,但是ROS1主要是存在于肺腺癌中。
5 `6 p% c7 \4 GROS1基因与其他驱动基因突变是不共存的,一项涵盖1073个样本的研究表明ROS1与EGFR、ALK等突变互斥,没有发现他们共同存在。一项涵盖556个患者的研究也表明,使用免疫组化IHC检测ALK和ROS1,没有发现二者共存。后续有报道研究两名ROS1阳性的患者发现了EGFR突变,分别是L858R和19号外显子缺失突变。但是这些为个别案例,总体上肿瘤的驱动基因都是互相排斥的,因为肿瘤也不需要两种驱动基因驱动其增殖。
M) L) _+ r+ G& ^. b d1 \5 Z38 b, p2 b8 c7 X: a6 j2 @! t
治疗ROS1阳性的克唑替尼
7 A' l' O/ a" u$ m' q由于ROS1突变与ALK的相似性,研究者很容易想到使用ALK的抑制剂去尝试治疗ROS1的突变。2014年公布的临床研究数据表明,50名患者每日两次口服250mg克唑替尼,客观应答率(ORR)为72%,包含3例患者完全缓解(CR),33例患者部分缓解(PR)。相比ALK突变,ROS1患者使用克唑替尼的反应持续时间更长,达到17.6个月,中位无进展生存期(PFS)为19.2个月,因此专家推出克唑替尼对ROS-1的抑制要强于ALK,而且ROS1阳性突变的患者预后相对较好。
8 t7 Z) X1 g+ \# U6 P: _美国FDA于2016年3月11日批准将克唑替尼用于治疗ROS1突变的转移性非小细胞肺癌患者。也是第一个FDA批准的ROS1阳性的靶向药物。但是克唑替尼治疗ROS1阳性的患者也不可避免为会产生耐药,这些耐药原因包含ROS1基因上的一些点突变,如G2032R、L2155S、L2026M、G2101A、K2003I、L1951R等。其中ROS1的G2101A、L2026M和G2032R的肿瘤细胞系对Foretinib敏感,但是L2155S对于Foretinib仍然耐药。G2032R和L2155S细胞系对TAE684也是不敏感的。除去这两个药物外,卡博替尼(XL184)展示出与部分耐药位点的疗效,如图3,ROS1阳性克唑替尼耐药后的L2026M、L1951R和G2032R可以被卡博替尼所解决,对于ROS1阳性的患者来说这算是一个好的事情,虽然这些是细胞系的研究,但是希望还是有的。这些需要着重注意,基因检测报告需要仔细查询是否有这些耐药位点,这些耐药位点的释义和相应的意义。6 z; f# e _8 O' D
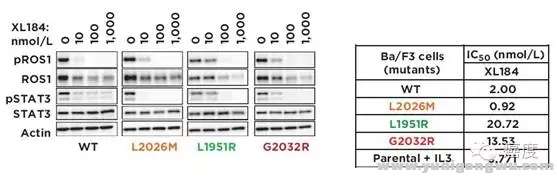
: x. m1 t/ |5 E3 e$ ~图3:ROS1的G2032等突变对卡博替尼敏感
; g6 k- b4 U% ~' L! x1 zROS1患者在克唑替尼使用的另一个耐药机制是EGFR的代偿性高表达(表达量为2.6倍),这个在肿瘤细胞系中获得了验证,同时使用EGFR的靶向药物吉非替尼或西妥昔单抗联合克唑替尼,可以起到协同抑制的作用(见图4)。
3 N9 X9 D6 M" W. ~! Q9 S( i! M, @
 ) v0 i. N4 S8 h# d8 i" k: F/ Z- X5 h6 ~
) v0 i. N4 S8 h# d8 i" k: F/ Z- X5 h6 ~
图4:克唑替尼联合达克替尼或阿法替尼,可控制部分ROS1患者的耐药
6 e! u# @# }. W) W/ a但是问题是,假如EGFR的高表达也确实是一部分ROS1患者的耐药原因,什么时候对患者进行检测呢,使用什么样本检测。检测的灵敏度和特异性如何?
* K% G# b1 b4 h2 b钙粘附蛋白E表达量丢失,波形蛋白和人纤维连接蛋白表达增加是另外一种ROS1阳性患者对克唑替尼耐药的原因。这导致细胞形态,以及细胞之间的粘附力出现改变。
9 O3 f1 ~6 T; ^! R, [2 k$ v3 d' U
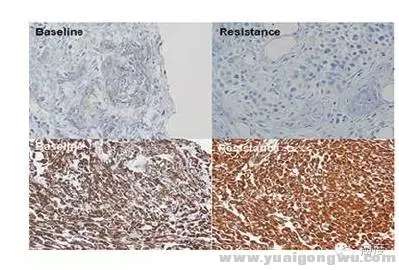
$ Q# `* M$ d' f图5:一些蛋白表达降低或升高也影响ROS1患者对克唑替尼的敏感性
% h j0 T0 y& T% y5 U另外也有文献报道KRAS、NRAS等也对ROS1阳性的患者使用克唑替尼耐药,从肿瘤细胞的进化考虑,ROS1对克唑替尼的耐药原因会是比较复杂的,也比较难以预测。因此究竟是什么原因耐药,一定要彻底进行检测明确。推荐什么类型的靶向药物,必须有一定的文献或临床数据支持。
7 s0 U9 ~' e+ m2 d9 Z: V4 t: o6 ]$ q" @
其他ROS1融合阳性的靶向药物
9 C L }+ W& v8 EALK和ROS1的激酶活性区域有70%的相似性,因此ALK的抑制剂很多是可以用于ROS1的治疗的,克唑替尼这个药物也就是这么误打误撞地搞出来的。其他的ALK抑制剂是否也可以呢?答案是有抑制效果但不都是。+ J) a2 M( j% s$ _' P' z* T
 , r' F, ?; W" q8 M: e' M5 X% V b$ q
, r' F, ?; W" q8 M: e' M5 X% V b$ q
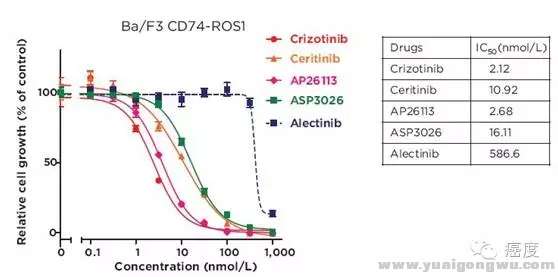
图6:ALK抑制剂对ROS1-CD74融合基因的抑制情况
1 q+ m3 t' `! c# u在图1上我们可以知道CD74是ROS1的主要融合伴侣基因,所以表达该融合基因的细胞系被用来测试ALK的抑制剂。从图6我们可以看出,克唑替尼、色瑞替尼(LDK378)、AP26113对ROS1-CD74的抑制效果很不错。ASP3026具有中度的抑制效果,艾乐替尼(CH5424802)没有显示出具有抑制活性,这个是为主要注意的,因为艾乐替尼在ALK中和克唑替尼的头对头临床试验效果很好,但是这并不能完全复制到ROS1阳性的患者上,最起码不能复制到CD74-ROS1的融合突变的患者上。* b3 x+ p5 K+ I' V3 o9 |8 y" {8 {
很多病友都熟悉3922这个ALK抑制剂,有资料称这个药物对于ROS1的抑制力度比克唑替尼强几十倍。我们查询了很多的文献,终于找到了一篇3922对ROS1的报道,给大家呈上。3 j( E3 O3 O) M& [$ k, B# k5 M: n8 O
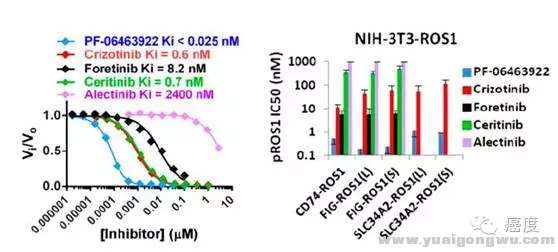
+ }# Z/ S+ \6 C! V# B! o) t; R0 d" Z图7:不同ALK抑制剂对ROS1的抑制活性,3922最优
7 g( y4 ]+ F7 c* c1 z. J$ a0 ]% N从图7中我们可以再次了解ALK抑制剂对ROS1突变的抑制活性,其实3922可以说是一骑绝尘。当然在这里我们再一次看到艾乐替尼对ROS1抑制不力,这个是需要着重注意的,不是所有的ALK抑制剂对ROS1都能起到好的抑制效果。
+ ?7 }# G: R$ [/ f对于ROS1突变导致的克唑替尼耐药,体外实验表明3922可以ROS1基因上的G2032R突变、G2026M突变具有抑制效果。在动物模型的体内实验上,3922对于FIG-ROS1、CD74-ROS1和存在G2032R耐药突变的CD74-ROS1都具有抑制活性。另外对于FIG-ROS1阳性胶质母细胞瘤的老鼠上也展示出抑制效果。这里需要注意ROS1有多个耐药突变,目前报道的是其中两种是可以用3922控制的,当然这是动物实验,后续仍需要进行跟踪了解。
4 t2 r9 g- V- R6 K! @7 i3 ?我们就本帖进行一次重点总结:$ C' o; H' a3 B( q5 B, C
ROS1的突变频率不是很高,在非小细胞肺癌里的频率仅为2%左右,但是目前有靶向药物克唑替尼批准。需要明确的是ROS1的突变形式是与其他基因发生融合。但是ROS1本身会产生一些耐药突变对克唑替尼耐药,这些耐药位点可以被其他靶向药物所解决,如卡博替尼、3922等。目前ROS1在其他癌种也有发现,但是跨癌种用药的疗效如果目前没有较为全面的报道,有胶质母细胞瘤脑的ROS1阳性老鼠对3922敏感。其他癌种如果检测出来ROS1阳性,且没有获准的靶向药物,跨癌种用药也是可以考虑的。; F$ V( ?: M- [6 V; s# X0 N, K/ Z* [9 C
小编的重要总结0 k" i6 D' ^. W. A, N+ q) |
1 v4 L9 ` P& S5 _) ^% t L- T
参考文献:
" K0 ^0 x. ?* x1 g$ X- @1、Kurtis D. Davies, et al., Clin Cancer Res. 2013 August 1; 19(15): 4040–4045.' R- L" ]0 E/ a1 ?( x$ H( t( t# j4 e' s$ D
2、Gainor JF, et al., Oncologist. 2013;18(7):865-75.9 H# G+ }3 ]! L u- E
3、Song A,et al.,Clin. Cancer Res. 21, 2379–2387(2015).
- _" ]% u q2 c5 a* z) m4、Katayama R, et al.,Clin Cancer Res. 2015 Jan 1;21(1):166-74
/ y/ V8 i0 V9 c Z6 d6 W5、Zou HY, et al., Proc Natl Acad Sci U S A. 2015 Mar 17;112(11):3493-8. |